學會會訊 2019 - 03
2019-06-29~2019-06-30

本屆華夏論壇主題為「亞太地區循證衛生政策:價值框架與證據應用」,在中國古都南京舉辦。與初屆華夏論壇僅有數十人與會相比,本屆論壇已有超過850位各國產官學界代表共襄盛舉,也一併見證了醫藥科技評估(health technology assessment, HTA)近年來在衛生政策的蓬勃發展。
整體而言,本次論壇讓筆者最印象深刻的是:中國政府在HTA的投入及迅速發展。本屆華夏論壇首場主題演說之講者,中國醫療保險研究會的王東進會長,開場即明確指出中國健康政策目標是實施健康中國2030戰略(2016年10月發布)以完善國民健康,其中藥物經濟學及醫藥科技評估是重要政策工具,希望在實證基礎上,公開、公平、公正地評價新醫療科技,以平衡醫療科技帶來之價值和花費的成本。為了達到此政策目標,需加強建置國內HTA之學習環境及人才庫,同時要促進國際交流,藉由學習他國經驗,整合國內資源以求思想上的創新。緊接著,中國國家衛生健康委員會藥物政策及基本藥物制度司(2018年成立)的張峰副司長全面地介紹了中國國家藥物政策,內容提及中國將針對基本藥物進行臨床價值評價,綜合分析藥品的安全性、有效性、經濟性、創新性、適宜性及可近性等六大構面,優先納入有效、安全及符合成本效益的藥品,並預計在2023年之前完善整個制度。隨後,國家衛生健康委發展研究中心的趙琨研究員介紹了中國HTA綜合評價之工作體系、評價內容及方法,包含主題遴選、項目管理(具有獨立資金的國家評估中心負責)、評估維度、評估內容及指標、數據來源、評估流程及評估結果的審閱及應用等,都有清楚及完整的介紹。
筆者參加本屆華夏論壇的感想是:中國之HTA雖然起步較晚,但HTA的資金和相關規章皆迅速到位,令人驚嘆其傾國家之力投入後的成果。在回頭看台灣的HTA發展,迄今仍未成立獨立財源之國家HTA中心;希冀政府盡早將國家HTA的發展當成施政的重點項目,並系統性地培育國內的HTA人才,以提升台灣整體醫療照護的品質。
整體而言,本次論壇讓筆者最印象深刻的是:中國政府在HTA的投入及迅速發展。本屆華夏論壇首場主題演說之講者,中國醫療保險研究會的王東進會長,開場即明確指出中國健康政策目標是實施健康中國2030戰略(2016年10月發布)以完善國民健康,其中藥物經濟學及醫藥科技評估是重要政策工具,希望在實證基礎上,公開、公平、公正地評價新醫療科技,以平衡醫療科技帶來之價值和花費的成本。為了達到此政策目標,需加強建置國內HTA之學習環境及人才庫,同時要促進國際交流,藉由學習他國經驗,整合國內資源以求思想上的創新。緊接著,中國國家衛生健康委員會藥物政策及基本藥物制度司(2018年成立)的張峰副司長全面地介紹了中國國家藥物政策,內容提及中國將針對基本藥物進行臨床價值評價,綜合分析藥品的安全性、有效性、經濟性、創新性、適宜性及可近性等六大構面,優先納入有效、安全及符合成本效益的藥品,並預計在2023年之前完善整個制度。隨後,國家衛生健康委發展研究中心的趙琨研究員介紹了中國HTA綜合評價之工作體系、評價內容及方法,包含主題遴選、項目管理(具有獨立資金的國家評估中心負責)、評估維度、評估內容及指標、數據來源、評估流程及評估結果的審閱及應用等,都有清楚及完整的介紹。
筆者參加本屆華夏論壇的感想是:中國之HTA雖然起步較晚,但HTA的資金和相關規章皆迅速到位,令人驚嘆其傾國家之力投入後的成果。在回頭看台灣的HTA發展,迄今仍未成立獨立財源之國家HTA中心;希冀政府盡早將國家HTA的發展當成施政的重點項目,並系統性地培育國內的HTA人才,以提升台灣整體醫療照護的品質。


2019-08-27

「真實世界資料(real world data, RWD)」、「真實世界證據(real world evidence, RWE)」到底是什麼?如何將RWD轉化為RWE?RWE對藥物發展的影響是什麼?近年來,RWD及RWE成為政府、業界和學界熱烈討論的議題,因為從真實世界所蒐集到的資料經過適當轉化為真實世界證據後,可以提供新藥開發、藥證審查及醫療科技評估的相關背景知識,但也有可能因此而影響到產業發展,故需要集思廣益蒐集更多的想法與建議,更謹慎地與各界討論。在本次的工作坊中,TaSPOR邀請四位國內外產學界的專家,各自分享專業領域上的經驗。
首先登場的是台北醫學大學的蒲若芳博士,演講題目為「Generating RWE from RWD: Experiences from Taiwan」,蒲博士以C肝防治為例說明如何從RWD轉化為RWE,進而形成政府的政策。蒲博士說明政府的目標是2025年消除國人的C肝疾病,在決策過程中需要評估有多少潛在的病人需要被治療以及國家財政能否負擔,而透過真實世界的數據可以得到需要治療的病人數,再輔以每人的療程費用便可以得知整體的財務影響。另外,治療C肝的直接作用抗病毒藥物(direct-acting antiviral agent, DAA)藥物於臨床試驗中的療效極佳,但在使用在真實世界後的療效是否等同臨床試驗,也可以透過RWD進行治療成效驗證。
接著登場的是Kantar Taiwan的林慧淳總經理,演講題目為「The Growing Importance of Patient Preference Studies: What, When, How and Why」,林總經理從自身的經驗來說明病人偏好(patient preference)對於新藥開發的重要性,並引用美國FDA的定義說明病人偏好是對病人相對需求或可接受性的量性或質性評估,這些結果涉及病人指定的替代方案或其他替代性健康介入措施之間不同的選擇偏好。由於病人是各類醫藥產品的最終使用者,病人偏好即是病人在成本、療效、風險三者間抉擇的結果,所以病人的用藥便利性、治療可選擇性、對生活品質的影響等因素,在藥物發展過程扮演舉足輕重的角色,而各種以病人偏好為主所進行的相關研究逐漸增加,對RWE的重要性也日益提高。
第三位講者是Kantar Health的腫瘤部門副總裁Dr. Otavio Clark,演講主題為「Putting Real World Evidence to Work in the Real World」,Dr. Clark說明RWD為除了臨床試驗研究資料外的各種觀察性研究資料,來源包括電子健康紀錄、保險申報及帳單資料、登錄資料等,而RWE便是透過各種工具將RWD整理為具結構性的有用資訊。由於RWD來自不同的個體,具有很高的異質性,資料蒐集方法設計便顯得相當重要,方能收集到有用的資訊。而轉化為RWE則可以借助人工智慧(artificial intelligence, AI)工具有效率地進行,如機器學習(machine learning)及自然語言處理(natural language processing, NLP)等;亦可以使用傾向分數配對(propensity score matching, PSM)方法以建立類似臨床試驗的可比較族群。
壓軸登場的講者是賽諾菲公司全球健康經濟暨價值評估商業夥伴的Dr. Indira Umareddy,演講主題為「Use of RWE to Optimize Access and Value of Innovative Medicines」,Dr. Umareddy引述自身經驗說明如使用RWE優化創新藥物的評估及價值,由於人口老化的因素,未來的健康照護花費將水漲船高,預計到2022年全球的健康照護花費將會達到10兆美金,如何將RWD轉化為RWE,以瞭解現行治療上的缺口及病人的需求,進而提昇新藥的價值,是製藥產業未來重要的課題之一。Dr. Umareddy舉出六個國家(日本、美國、法國、英國、德國、丹麥)為例說明可用的RWD來源,並分別以製藥產業觀點及HTA觀點分享RWE應用的成果。
在這次的工作坊中,聽到來自不同角度對於RWD及RWE的觀點及應用結果,我國擁有超過20年的健保資料庫,也有癌症登記檔、死因檔、國民健康訪問調查等資料庫,累積了許多的真實世界資料,如何能將這些真實世界資料轉化成有用的真實世界證據,進而提供產、官、學界運用於相關領域的發展,有賴各界共同努力從RWD礦山中開採出璀璨的RWE寶石。
首先登場的是台北醫學大學的蒲若芳博士,演講題目為「Generating RWE from RWD: Experiences from Taiwan」,蒲博士以C肝防治為例說明如何從RWD轉化為RWE,進而形成政府的政策。蒲博士說明政府的目標是2025年消除國人的C肝疾病,在決策過程中需要評估有多少潛在的病人需要被治療以及國家財政能否負擔,而透過真實世界的數據可以得到需要治療的病人數,再輔以每人的療程費用便可以得知整體的財務影響。另外,治療C肝的直接作用抗病毒藥物(direct-acting antiviral agent, DAA)藥物於臨床試驗中的療效極佳,但在使用在真實世界後的療效是否等同臨床試驗,也可以透過RWD進行治療成效驗證。
接著登場的是Kantar Taiwan的林慧淳總經理,演講題目為「The Growing Importance of Patient Preference Studies: What, When, How and Why」,林總經理從自身的經驗來說明病人偏好(patient preference)對於新藥開發的重要性,並引用美國FDA的定義說明病人偏好是對病人相對需求或可接受性的量性或質性評估,這些結果涉及病人指定的替代方案或其他替代性健康介入措施之間不同的選擇偏好。由於病人是各類醫藥產品的最終使用者,病人偏好即是病人在成本、療效、風險三者間抉擇的結果,所以病人的用藥便利性、治療可選擇性、對生活品質的影響等因素,在藥物發展過程扮演舉足輕重的角色,而各種以病人偏好為主所進行的相關研究逐漸增加,對RWE的重要性也日益提高。
第三位講者是Kantar Health的腫瘤部門副總裁Dr. Otavio Clark,演講主題為「Putting Real World Evidence to Work in the Real World」,Dr. Clark說明RWD為除了臨床試驗研究資料外的各種觀察性研究資料,來源包括電子健康紀錄、保險申報及帳單資料、登錄資料等,而RWE便是透過各種工具將RWD整理為具結構性的有用資訊。由於RWD來自不同的個體,具有很高的異質性,資料蒐集方法設計便顯得相當重要,方能收集到有用的資訊。而轉化為RWE則可以借助人工智慧(artificial intelligence, AI)工具有效率地進行,如機器學習(machine learning)及自然語言處理(natural language processing, NLP)等;亦可以使用傾向分數配對(propensity score matching, PSM)方法以建立類似臨床試驗的可比較族群。
壓軸登場的講者是賽諾菲公司全球健康經濟暨價值評估商業夥伴的Dr. Indira Umareddy,演講主題為「Use of RWE to Optimize Access and Value of Innovative Medicines」,Dr. Umareddy引述自身經驗說明如使用RWE優化創新藥物的評估及價值,由於人口老化的因素,未來的健康照護花費將水漲船高,預計到2022年全球的健康照護花費將會達到10兆美金,如何將RWD轉化為RWE,以瞭解現行治療上的缺口及病人的需求,進而提昇新藥的價值,是製藥產業未來重要的課題之一。Dr. Umareddy舉出六個國家(日本、美國、法國、英國、德國、丹麥)為例說明可用的RWD來源,並分別以製藥產業觀點及HTA觀點分享RWE應用的成果。
在這次的工作坊中,聽到來自不同角度對於RWD及RWE的觀點及應用結果,我國擁有超過20年的健保資料庫,也有癌症登記檔、死因檔、國民健康訪問調查等資料庫,累積了許多的真實世界資料,如何能將這些真實世界資料轉化成有用的真實世界證據,進而提供產、官、學界運用於相關領域的發展,有賴各界共同努力從RWD礦山中開採出璀璨的RWE寶石。

小芳老師碎碎念-TaSPOR篇系列4


再談早期感知與預警系統
楊雯雯理事
今年6月在台灣衛誌出刊了一篇「從英國發展早期感知與預警系統的經驗為例,看台灣健康照護體系之應用」在介紹前瞻性評估(horizon scanning),近年或稱為早期感知與預警系統(early awareness and alert [EAA] system),由於偏向學術論述性質,太過咬文嚼字,每每和蒲老師與吳慧敏博士聊起來,就覺得有些話還沒講清楚,於是就藉著喝咖啡的時間一吐心中之快。
Horizon scanning 和EAA system
英國衛生照護系統早自1997起即開始發展「新與新興(new and emerging)」醫療科技的前瞻性評估(horizon scanning [或稱為水平掃描] ),隔年正式成為國家衛生研究院(National Institute for Health Research, NIHR)下的計畫單位–科技偵測與情報中心(Horizon Scanning Research and Intelligence Centre, HSRIC),並獲得國家公共資金的挹注,以因應新與新興醫療科技進入照護系統所需的法規、財務衝擊、環境建置、人力培訓、倫理考量等事宜,便於相關單位機構能預做安排與規劃。隨全球創新科技日新月異的發展,為提升英國在高齡、數位導向產品與服務研發能量,促進未來醫療科技的研發,應用大數據分析方法學於加速新醫藥科技引入與使用,2017年更將前瞻性評估機構轉型與擴大為NIHR創新觀測中心(Innovation Observatory, IO)。
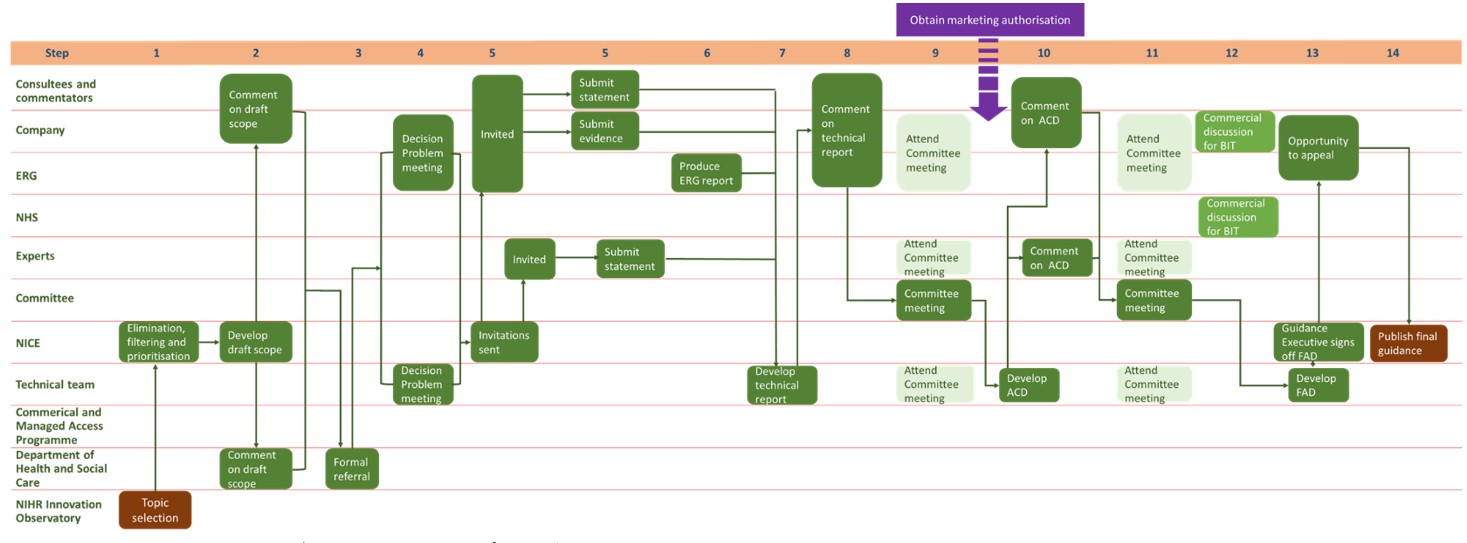
無論是NIHR HSRIC或是NIHR IO,都有一項任務是要主動提供英國衛生和社會照護部(Department of Health and Social Care, DHSC)與健康服務決策體系推估當下3年內可能會用於英國國民健康服務(National Health Service, NHS)的重要新與新興健康科技資訊(Filtration Form和Briefing),而且這些新科技極有必要進一步被評估,包括臨床與成本效果、成本對NHS的影響、臨床在採用該技術時所必要的相關需求、或該技術在NHS內採用時須修改臨床診療指引的可能性。當確認主題(topic selection, TS)之後,將啟動一連串的國家健康暨照護卓越研究院(National Institute for Health and Care Excellence, NICE)科技評價(technology appraisal, TA)流程,最終形成科技評價指引(TA guidance)。科技評價流程步驟與所涉及的相關機構或人員關係,簡繪於圖一。從圖一可見NIHR IO(圖一左下角磚紅色方框)的任務僅為科技評價(TA)的開端,後續尚有諸多程序,以及諸多利害關係人(stakeholder)的投入與付出才能成就一份科技評價指引(圖一右下角磚紅色方框)。
Horizon scanning 和EAA system
英國衛生照護系統早自1997起即開始發展「新與新興(new and emerging)」醫療科技的前瞻性評估(horizon scanning [或稱為水平掃描] ),隔年正式成為國家衛生研究院(National Institute for Health Research, NIHR)下的計畫單位–科技偵測與情報中心(Horizon Scanning Research and Intelligence Centre, HSRIC),並獲得國家公共資金的挹注,以因應新與新興醫療科技進入照護系統所需的法規、財務衝擊、環境建置、人力培訓、倫理考量等事宜,便於相關單位機構能預做安排與規劃。隨全球創新科技日新月異的發展,為提升英國在高齡、數位導向產品與服務研發能量,促進未來醫療科技的研發,應用大數據分析方法學於加速新醫藥科技引入與使用,2017年更將前瞻性評估機構轉型與擴大為NIHR創新觀測中心(Innovation Observatory, IO)。
無論是NIHR HSRIC或是NIHR IO,都有一項任務是要主動提供英國衛生和社會照護部(Department of Health and Social Care, DHSC)與健康服務決策體系推估當下3年內可能會用於英國國民健康服務(National Health Service, NHS)的重要新與新興健康科技資訊(Filtration Form和Briefing),而且這些新科技極有必要進一步被評估,包括臨床與成本效果、成本對NHS的影響、臨床在採用該技術時所必要的相關需求、或該技術在NHS內採用時須修改臨床診療指引的可能性。當確認主題(topic selection, TS)之後,將啟動一連串的國家健康暨照護卓越研究院(National Institute for Health and Care Excellence, NICE)科技評價(technology appraisal, TA)流程,最終形成科技評價指引(TA guidance)。科技評價流程步驟與所涉及的相關機構或人員關係,簡繪於圖一。從圖一可見NIHR IO(圖一左下角磚紅色方框)的任務僅為科技評價(TA)的開端,後續尚有諸多程序,以及諸多利害關係人(stakeholder)的投入與付出才能成就一份科技評價指引(圖一右下角磚紅色方框)。
NIHR IO在協助DHSC決定某項新醫療科技是否納入NHS體系的目的下,會根據早期感知與預警(early awareness and alert, EAA)步驟初步篩選出適合進行TA的新科技議題,特別是預計距上市時間還有20個月的新藥(新增適應症藥品則是距離新適應症獲得核可前15個月),以便讓NICE發布該產品TA報告的時間儘可能與上市時間相近(取得英國上市許可日起之90天內)。NIHR IO每隔幾週會將其彙整的新醫療科技簡扼摘要表(Filtration Form)遞送給NICE的主題選擇小組(topic selection team, TS)。TS成員包括衛生部政策小組、NHS委員、健康醫療照護專家等,TS工作人員初步會依據公告的篩選標準過濾各項新醫療科技主題,然後提供給TS成員以決定需要進一步評估的候選新醫療科技,當TS成員對新醫療科技候選主題產生共識,將進一步請NIHR IO提供10頁以內的摘要報告(Briefing)。Briefing內容包括目標新科技的介紹、未來使用目標群、該科技之創新處和優點、當下之研發階段、是否符合NHS或政府優先策略、臨床需求和疾病負擔、現有相關指引、現有治療選擇、該科技之臨床試驗及結果、洽廠商訪價後的初略成本費用估算、未來預計會影響的層面等,交由TS再依篩選標準和優先執行標準建立待評估主題清單,並請NICE科技評價(TA)範疇界定小組界定評估的範疇(scoping)。前述內容部分已刊載於台灣衛誌第38卷第3期236-251頁。
重點不在精準預算規劃!
雖然執行EAA的目標之一,是要輔助健康照護系統內的相關組織機構為即將進入照護系統的新醫療科技預行財務影響評估與安排,但不可諱言的,EAA並不是用來做為精準預測預算額度的工具,否則英國NHS就不會年年都在面對經費短絀與超支的事實。NHS面對新藥物的成本持續增長,一方面被期待維護藥物的價值,一方面又要促進治療的可近性,導致得規劃更多的預算來因應NICE建議的科技評價項目,於是英國衛生照護系統也做了一些功課來管理藥物的預算增長,除了既有的預算與支出審查及修正機制外,長期以來,DHSC與英國製藥工業協會(Association of the British Pharmaceutical Industry, ABPI)一起發展彈性的藥價機制,利用商業經營的靈活性概念,發展諸如簡單型與複雜型保密折扣(confidential discount)、病人用藥可近性方案(patient access scheme)、藥品近用管理協議(managed access agreement)、建立收集新藥物使用病人高品質數據的辦法、保密商業協議(confidential commercial arrangement)等各式協議,透過可用的商業選項,逐案決定適合產品特質的商業靈活協議方案,如此一來既可維持個別新藥在NHS的檯面價(list price),又可解決該藥物在不確定性、價值、可負擔性和風險上的爭議,不過在協商採取可能的方案之前,過於複雜方案的管理與執行對於各方都可能會占用大量的資源,因此NHS仍會考量各方案對NHS造成的總體負擔,再決定協議的類型與內容。
新的方法– EAMS
DHSC為了提供具威脅生命或導致嚴重衰弱疾病者,有機會使用明確具有未滿足醫療需求且尚未取得上市許可的藥物,於是在2014年4月提出藥物早期近用方案(Early Access to Medicines Scheme, EAMS)。EAMS是由英國藥物及保健產品管理局(Medicines and Healthcare Products Regulatory Agency, MHRA)、NHS和該藥品持有商一起合作,讓進入查驗登記程序後期階段,且取得潛力創新藥品認定的藥物,能在該藥物正式取得上市許可前的12至18個月左右,就讓病人有機會使用。(有機會再來詳細介紹)
NICE評價過程終也加入BIA
由於NICE長期以來在審議科技評價項目時並未以NHS的財務負擔為要點,但漸增的新藥費用不得不讓NHS委託服務委員會(Commissioning Board, CB)直接建議NICE在草擬科技評價指引時,應該將NHS的可負擔性和勞動力納入評估考量。於是自2017年4月1日起,NICE在科技評價(TA)計畫和高度專業科技評估計畫(Highly Specialised Technology [HST] Evaluation Programme)執行新醫療科技評價時,導入預算影響測試(budget impact test)方法學,針對擬進入NHS使用的藥物進行前3個財政年度的財務影響評估。如果在3年中任一年的預算影響超過2千萬英鎊,NHS有可能邀請該藥物持有商做進一步的商業性討論,以減緩屆時NHS使用該藥物的預算影響,萬一雙方討論結果無法形成商業性協議,則NHS也有機會提出更改法定資金的需求。
在收到持有商提交的資料後,NICE將在17個日曆天內完成該藥物潛在預算影響評估,並通知NHS和持有商是否其中任一年的淨預算會超過2千萬英鎊。NHS在收到通知的7天內,必須告訴NICE是否要跟持有商進行商業討論,以便讓NICE人員可以變更科技評價的時程表。預算影響的商業性討論與科技評價是同步進行的,故此NHS必須至少在首次評價委員會會議(committee meeting)開議前7個日曆天通知NICE商業協議討論的最新情況。當評價委員會會議決定將該藥物做為NHS使用的選項,或是最佳條件下使用的建議時,NICE將更新該預算影響評估,然後通知NHS和持有商,同時發布評價諮詢文件(appraisal consultation document, ACD)或是最終評價文件(final appraisal document, FAD)。若NHS和持有商有意進行商業性近用協議(commercial access agreement),NHS必須在接到更新預算影響評估資料後7個日曆天內通知NICE,好讓NICE人員安排暫停評價程序(最多暫停12週),並通知科技評價的被徵詢意見者(consultees)和評論者(commentators),第二次的committee meeting將視商業參與的進展重新安排。若評價委員會決定更改評價建議,NICE便進行預算影響更新評估,並在FAD發布時也通知NHS和持有商更新結果。此間,若NHS打算申請變更法定資金需求,則應盡早提出,不遲於consultees、commentators、或是持有商提出申訴的最終期限。
BIA不只講藥費
NICE資源影響團隊(resource impact team, RIT)的任務,在估計執行科技評價和高度專業科技評估指引所涉及的成本和節省情況,雖然以財務為主,但也評估勞動力、容量與需求、基礎建設、訓練與教育等面向。當初步科技評價結果是建議要使用時(positive recommendation),RIT會利用資源規劃工具(resource planner)協助NHS和臨床醫療委託小組(clinical commissioning group, CCG)理解該藥物在NHS內使用的預算影響是低、中、或高的可能性,不過如果價格被列為機密,則預算影響估算將不會被公開揭露。RIT對資源影響的定義如下:
EAA對NHS新藥總預算估算的貢獻有限
在英國獲得第一個適應症許可的新成分新藥(New Active Substances)在取得上市許可後之36個月內享有自由定價的權利,若持有商打算在英國販售,可能的話甚至希望該藥物在NHS內使用的話,則持有商需要將其list price通知DHSC。此外製藥業亦被鼓勵登錄所持有的藥物相關資訊到UK PharmaScan,以提供英國所有執行EAA和HTA評估相關組織獲得更為完整和精確的訊息,包括產品資訊、用法、用量、可能的比較品、臨床試驗、法規送審進度、成本等(參見台灣衛誌第38卷第3期236-251頁內容)。英國執行EAA的單位是以主動的方式來收集並辨識新醫療科技,無論是執行EAA或是HTA的單位,除透過UK PharmaScan了解新醫療科技的資訊外,與廠商之間也維持有通暢的溝通管道,以利於更新相關的異動,因此對於藥物價格、上市時程、NICE委員會會議時程都有較高的掌控度,對於NHS預算規劃也有機會提出變更。
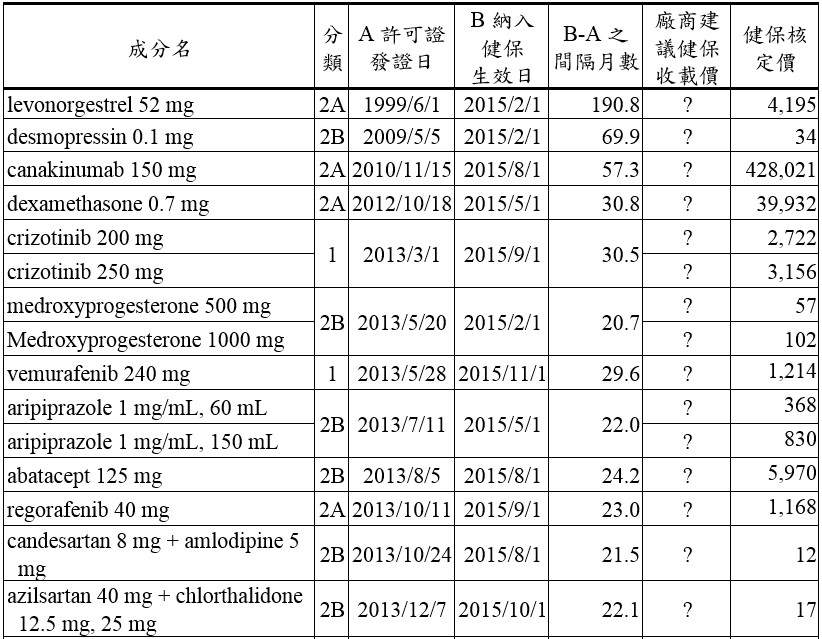
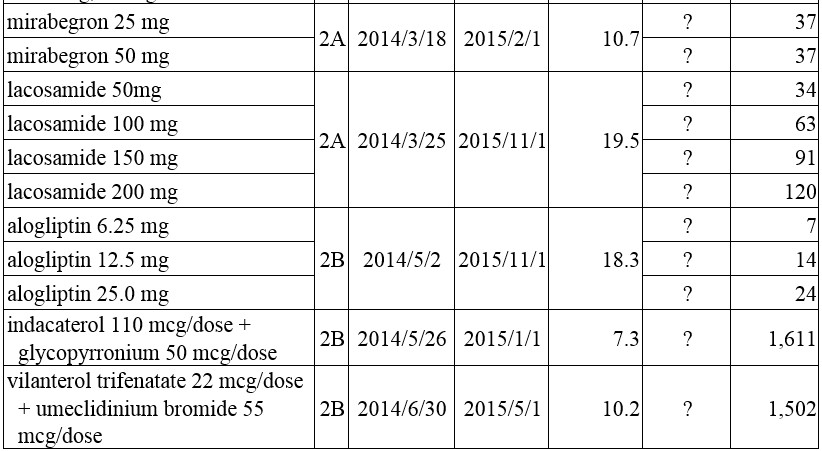
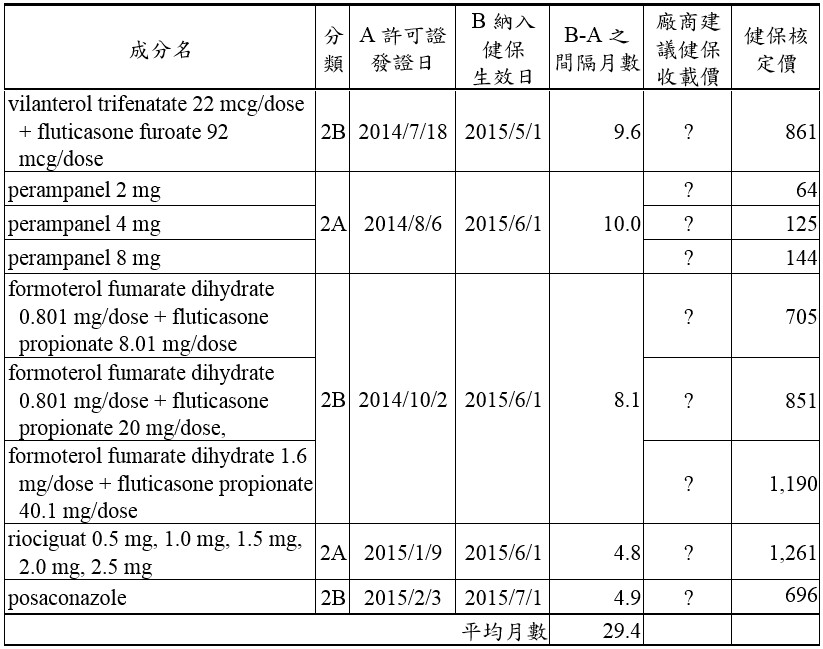
應用EAA方法學於新或新興醫療科技的挑戰,包括如何獲得機密性數據(如售價)、目標族群有可能難以定義或量化、查登前臨床試驗階段的時程縮短、查驗登記審查延遲、評估的適應症最終可能與許可的適應症不同、市占率難以估計等困難。英國NIHR IO選擇藥物主題階段所提供的新藥物成本和參考品成本,僅為後續NICE進行科技評價的參考來源之一,要減緩對NHS的預算衝擊,NICE方面則由不同的單位在協助NHS的預算影響估算與發展商業協議。對我國而言,前揭挑戰具存,以2015年納入健保收載的22種主成分新藥為例,縱使不考量得從獲得許可證前多少個月就導入EAA方法,就從取得許可證當下的新藥來評估,從表一即可觀察到,許可證發證日至納入健保生效日間隔了4.8個月至190.8個月,平均29.4個月。這般的差距到底是源自持有商不全急於建議健保收載,或是卡在提出建議案至健保共同擬訂會議程序間的哪一個部分,或是還有其他原因不得而知,至少利用剛獲得許可證的藥物來匡列新醫療科技之新藥預算恐有極大的不確定性,遑論此階段更無法預測生效日的核定價格。再者,新藥納入健保後,常態上係自第2年才呈現用量的大幅上升,僅以英國EAA方法或現階段以提交建議案當時的藥價與目標量來預估生效日後的年度預算影響亦有不切實際之憂,更有趣的是,健保整體總額一年高達7千多億元,總藥費也近2千億點,我們卻糾結在40億左右的新醫療科技預算,甚至耗費諸多的精力只為在每一件新藥預算影響估算中,找出為何與實際支出有落差的原因。我國應該以自有的健保收載與實務操作為基礎,考量總額預算範圍之規劃、分配、執行等時程,以及現行藥物給付項目及支付標準之價格訂定原則和藥品給付協議等管理手段,來修正並建立適合我國執行面且務實的新醫療科技預算編列方法。
表一、2015年納入健保收載之新藥
重點不在精準預算規劃!
雖然執行EAA的目標之一,是要輔助健康照護系統內的相關組織機構為即將進入照護系統的新醫療科技預行財務影響評估與安排,但不可諱言的,EAA並不是用來做為精準預測預算額度的工具,否則英國NHS就不會年年都在面對經費短絀與超支的事實。NHS面對新藥物的成本持續增長,一方面被期待維護藥物的價值,一方面又要促進治療的可近性,導致得規劃更多的預算來因應NICE建議的科技評價項目,於是英國衛生照護系統也做了一些功課來管理藥物的預算增長,除了既有的預算與支出審查及修正機制外,長期以來,DHSC與英國製藥工業協會(Association of the British Pharmaceutical Industry, ABPI)一起發展彈性的藥價機制,利用商業經營的靈活性概念,發展諸如簡單型與複雜型保密折扣(confidential discount)、病人用藥可近性方案(patient access scheme)、藥品近用管理協議(managed access agreement)、建立收集新藥物使用病人高品質數據的辦法、保密商業協議(confidential commercial arrangement)等各式協議,透過可用的商業選項,逐案決定適合產品特質的商業靈活協議方案,如此一來既可維持個別新藥在NHS的檯面價(list price),又可解決該藥物在不確定性、價值、可負擔性和風險上的爭議,不過在協商採取可能的方案之前,過於複雜方案的管理與執行對於各方都可能會占用大量的資源,因此NHS仍會考量各方案對NHS造成的總體負擔,再決定協議的類型與內容。
新的方法– EAMS
DHSC為了提供具威脅生命或導致嚴重衰弱疾病者,有機會使用明確具有未滿足醫療需求且尚未取得上市許可的藥物,於是在2014年4月提出藥物早期近用方案(Early Access to Medicines Scheme, EAMS)。EAMS是由英國藥物及保健產品管理局(Medicines and Healthcare Products Regulatory Agency, MHRA)、NHS和該藥品持有商一起合作,讓進入查驗登記程序後期階段,且取得潛力創新藥品認定的藥物,能在該藥物正式取得上市許可前的12至18個月左右,就讓病人有機會使用。(有機會再來詳細介紹)
NICE評價過程終也加入BIA
由於NICE長期以來在審議科技評價項目時並未以NHS的財務負擔為要點,但漸增的新藥費用不得不讓NHS委託服務委員會(Commissioning Board, CB)直接建議NICE在草擬科技評價指引時,應該將NHS的可負擔性和勞動力納入評估考量。於是自2017年4月1日起,NICE在科技評價(TA)計畫和高度專業科技評估計畫(Highly Specialised Technology [HST] Evaluation Programme)執行新醫療科技評價時,導入預算影響測試(budget impact test)方法學,針對擬進入NHS使用的藥物進行前3個財政年度的財務影響評估。如果在3年中任一年的預算影響超過2千萬英鎊,NHS有可能邀請該藥物持有商做進一步的商業性討論,以減緩屆時NHS使用該藥物的預算影響,萬一雙方討論結果無法形成商業性協議,則NHS也有機會提出更改法定資金的需求。
在收到持有商提交的資料後,NICE將在17個日曆天內完成該藥物潛在預算影響評估,並通知NHS和持有商是否其中任一年的淨預算會超過2千萬英鎊。NHS在收到通知的7天內,必須告訴NICE是否要跟持有商進行商業討論,以便讓NICE人員可以變更科技評價的時程表。預算影響的商業性討論與科技評價是同步進行的,故此NHS必須至少在首次評價委員會會議(committee meeting)開議前7個日曆天通知NICE商業協議討論的最新情況。當評價委員會會議決定將該藥物做為NHS使用的選項,或是最佳條件下使用的建議時,NICE將更新該預算影響評估,然後通知NHS和持有商,同時發布評價諮詢文件(appraisal consultation document, ACD)或是最終評價文件(final appraisal document, FAD)。若NHS和持有商有意進行商業性近用協議(commercial access agreement),NHS必須在接到更新預算影響評估資料後7個日曆天內通知NICE,好讓NICE人員安排暫停評價程序(最多暫停12週),並通知科技評價的被徵詢意見者(consultees)和評論者(commentators),第二次的committee meeting將視商業參與的進展重新安排。若評價委員會決定更改評價建議,NICE便進行預算影響更新評估,並在FAD發布時也通知NHS和持有商更新結果。此間,若NHS打算申請變更法定資金需求,則應盡早提出,不遲於consultees、commentators、或是持有商提出申訴的最終期限。
BIA不只講藥費
NICE資源影響團隊(resource impact team, RIT)的任務,在估計執行科技評價和高度專業科技評估指引所涉及的成本和節省情況,雖然以財務為主,但也評估勞動力、容量與需求、基礎建設、訓練與教育等面向。當初步科技評價結果是建議要使用時(positive recommendation),RIT會利用資源規劃工具(resource planner)協助NHS和臨床醫療委託小組(clinical commissioning group, CCG)理解該藥物在NHS內使用的預算影響是低、中、或高的可能性,不過如果價格被列為機密,則預算影響估算將不會被公開揭露。RIT對資源影響的定義如下:
- 低於0英鎊-節省成本
- 高至5百萬英鎊-低成本或不重要
- 5百萬至2千萬英鎊-中成本
- 2千英鎊級以上-高成本
EAA對NHS新藥總預算估算的貢獻有限
在英國獲得第一個適應症許可的新成分新藥(New Active Substances)在取得上市許可後之36個月內享有自由定價的權利,若持有商打算在英國販售,可能的話甚至希望該藥物在NHS內使用的話,則持有商需要將其list price通知DHSC。此外製藥業亦被鼓勵登錄所持有的藥物相關資訊到UK PharmaScan,以提供英國所有執行EAA和HTA評估相關組織獲得更為完整和精確的訊息,包括產品資訊、用法、用量、可能的比較品、臨床試驗、法規送審進度、成本等(參見台灣衛誌第38卷第3期236-251頁內容)。英國執行EAA的單位是以主動的方式來收集並辨識新醫療科技,無論是執行EAA或是HTA的單位,除透過UK PharmaScan了解新醫療科技的資訊外,與廠商之間也維持有通暢的溝通管道,以利於更新相關的異動,因此對於藥物價格、上市時程、NICE委員會會議時程都有較高的掌控度,對於NHS預算規劃也有機會提出變更。
應用EAA方法學於新或新興醫療科技的挑戰,包括如何獲得機密性數據(如售價)、目標族群有可能難以定義或量化、查登前臨床試驗階段的時程縮短、查驗登記審查延遲、評估的適應症最終可能與許可的適應症不同、市占率難以估計等困難。英國NIHR IO選擇藥物主題階段所提供的新藥物成本和參考品成本,僅為後續NICE進行科技評價的參考來源之一,要減緩對NHS的預算衝擊,NICE方面則由不同的單位在協助NHS的預算影響估算與發展商業協議。對我國而言,前揭挑戰具存,以2015年納入健保收載的22種主成分新藥為例,縱使不考量得從獲得許可證前多少個月就導入EAA方法,就從取得許可證當下的新藥來評估,從表一即可觀察到,許可證發證日至納入健保生效日間隔了4.8個月至190.8個月,平均29.4個月。這般的差距到底是源自持有商不全急於建議健保收載,或是卡在提出建議案至健保共同擬訂會議程序間的哪一個部分,或是還有其他原因不得而知,至少利用剛獲得許可證的藥物來匡列新醫療科技之新藥預算恐有極大的不確定性,遑論此階段更無法預測生效日的核定價格。再者,新藥納入健保後,常態上係自第2年才呈現用量的大幅上升,僅以英國EAA方法或現階段以提交建議案當時的藥價與目標量來預估生效日後的年度預算影響亦有不切實際之憂,更有趣的是,健保整體總額一年高達7千多億元,總藥費也近2千億點,我們卻糾結在40億左右的新醫療科技預算,甚至耗費諸多的精力只為在每一件新藥預算影響估算中,找出為何與實際支出有落差的原因。我國應該以自有的健保收載與實務操作為基礎,考量總額預算範圍之規劃、分配、執行等時程,以及現行藥物給付項目及支付標準之價格訂定原則和藥品給付協議等管理手段,來修正並建立適合我國執行面且務實的新醫療科技預算編列方法。
表一、2015年納入健保收載之新藥



會議訊息分享

2019
11/2-11/6 ISPOR Europe 2019 (Copenhagen, Denmark)
2020
4/13-16 9th HTAsiaLink (Bali, Indonesia)
5/16-5/20 ISPOR 2020 (Orlando, FL, USA)
6/13-16 AcademyHealth 2020 Annual Research Meeting (Boston, MA, USA)
6/20-6/24 HTAi 2020 (Beijing, China)
8/26-30 36th ICPE (International Conference on Pharmacoepidemiology & Therapeutic Risk Management)
9/12-9/15 ISPOR Asia Pacific 2020 (Seoul, South Korea)
9/29-9/30 ISPOR Dubai 2020 (Dubai, United Arab Emirates)
10/15-17 ISPE’s 13th Asian Conference on Pharmacoepidemiology
11/14-11/18 ISPOR Europe 2020 (Milan, Italy)
11/2-11/6 ISPOR Europe 2019 (Copenhagen, Denmark)
2020
4/13-16 9th HTAsiaLink (Bali, Indonesia)
5/16-5/20 ISPOR 2020 (Orlando, FL, USA)
6/13-16 AcademyHealth 2020 Annual Research Meeting (Boston, MA, USA)
6/20-6/24 HTAi 2020 (Beijing, China)
8/26-30 36th ICPE (International Conference on Pharmacoepidemiology & Therapeutic Risk Management)
9/12-9/15 ISPOR Asia Pacific 2020 (Seoul, South Korea)
9/29-9/30 ISPOR Dubai 2020 (Dubai, United Arab Emirates)
10/15-17 ISPE’s 13th Asian Conference on Pharmacoepidemiology
11/14-11/18 ISPOR Europe 2020 (Milan, Italy)